Руководитель лаборатории — в.н.с., к.м.н. Московцев Алексей Александрович.
тел. 8-(499) 151-83-30
bioinf@mail.ru
Из истории лаборатории. Лаборатория клеточного стресса была сформирована 16 сентября 2024 года на базе группы клеточного стресса. В ней были продолжены исследования по трем ключевым направлениям: Стресс эндоплазматического ретикулума (ЭПР) и ЭПР-стресс-индуцированное старение; Биомоделирование с помощью микрофлюидных технологий — «сосуд-на-чипе»; Исследование эффектов микрогравитации на клеточном уровне.
Основные направления деятельности лаборатории и достижения.
Клеточный стресс – состояние клетки от начала действия нефизиологических факторов и начальных клеточных повреждений до адаптации или активации клеточной гибели. Под нефизиологическими понимаются факторы физической, химической, биологической (вирусы, бактерии), действие которых способно вызывать дисфункцию и повреждение клетки. Клетки в организме человека испытывают постоянное действие стрессорных факторов – физических, химических, вирусной природы. Клеточный стрессовый ответ — системная реакции клетки на резкое изменение условий ее функционирования, она включает в том числе активацию сложной последовательности экспрессии генов. Эта реакция универсальна для клеток всех типов, эволюционировала миллиарды лет и вовлечена в качестве базового механизма в большинство патологий, может рассматриваться как типовой патологический процесс. В ходе стрессового ответа клетка фактически «принимает решение» о своей дальнейшей «судьбе» — самоустраниться (апоптоз), адаптироваться, или постареть (см. ниже). Учитывая столь важную развилку, изучение механизмов регуляции клеточного стрессового ответа и поиск его модуляторов имеет ключевое значение для биомедицины.
Предложено определение клеточного стресса как не специфичной относительно вызвавшей причины реакции на любую форму макромолекулярного повреждения, превышающего пороговую величину (Dietmar Kültz, 2003). Цель стрессовой реакции – временное увеличение толерантности к повреждениям макромолекул посредством использования консервативных наборов генов и путей, которые опосредуют глобальную макромолекулярную стабилизацию и репарацию для обеспечения клеточной и организменной целостности в субоптимальных условиях (Dietmar Kültz, 2003). Этот механизм предоставляет время, необходимое для осуществления дополнительного набора специфичных адаптаций, направленных на восстановление клеточного гомеостаза.
Физиологическое клеточное старение понимается как необратимый арест роста, устойчивый к экзогенным митогенам. Ряд внешних и внутренних факторов, превышающих физиологический уровень и способных индуцировать клеточный стресс — таких, как активные формы кислорода, повреждение ДНК, дефицит нуклеотидов, активированные онкогены, цитокины,и др., вызывают так называемый стресс-индуцированный «преждевременный» тип старения, фенотипически сходный с репликативным.
Недавно нами было показано, что хронический стресс эндоплазматического ретикулума (ЭПР) – один из видов клеточного стресса, связанный с нарушением фолдинга белков в ЭПР – приводит к формированию фенотипа клеточного старения в фибробластоподобных клетках FRSN (Zaychenko et al., 2023). Несмотря на то, что острый стресс ЭПР способен снижать биогенез микроРНК (Mesitov et al, 2017), хронический стресс не приводит к существенному падению глобальной экспрессии микроРНК и сопровождается лишь незначительным снижением экспрессии мРНК DICERI (Zaychenko et al., 2023).
Инициирующие клеточное старение сигналы могут представлять собой повреждающиеся макромолекулы клеток. Не исключено, что эти повреждения могут способствовать перегрузке репарационных систем клетки. Может формироваться порочный круг, когда поломки могут распространяться на механизмы репарации и вызывать дальнейшее накопление повреждений. Клеточное старение может рассматриваться как альтернативный апоптозу выход клетки из цикла с сохранением жизнеспособности стареющих клеток в течение длительного времени, но с существенными изменениями клеточного фенотипа и механизмов взаимодействия с микроокружением, одним из наиболее существенных из них – провоспалительные сигналы, продуцируемые стареющими клетками. С учетом влияния, оказываемого стареющими клетками на гомеостаз, клеточное старение вовлечено в широкий спектр патологических процессов и имеет ключевое значение для патологической физиологии. Вместе с тем, процесс клеточного старения включает адаптивные изменения экспрессии генов – а эти механизмы зависят от множества РНК-регуляторов, действующих на транскрипционном и посттранскрипционном уровнях. Разработка РНК-модуляторов клеточного старения, направленных как на ускорение старения (например, для противоопухолевой терапии) или его замедление представляет собой перспективный подход, и разработка РНК-терапевтических препаратов будет способствовать эффективной борьбе с возрастассоциированными заболеваниями. В этой связи, это ключевое направление отражено в теме государственного задания, выполняемого в лаборатории: «РНК-опосредованная регуляция клеточного старения, индуцируемого факторами клеточного стресса: новые механизмы и разработка РНК-терапевтической платформы для возрастзависимых заболеваний».
Впервые были систематически изучены фрагменты транспортной РНК при хроническом стрессе эндоплазматического ретикулума и клеточном старении (Zaychenko et al., 2024). Впервые обнаружен ряд фрагментов тРНК – так называемых половинок тРНК, или tiRNA, представленных как в обоих клеточных состояниях, так и специфичных для хроничееского стресса и репликативного клеточного старения. Данные фрагменты участвуют во временном блокировании кеп-зависимой трансляции при клеточном стрессе, и могут играть важную роль в адаптации клеток к стрессу через инициацию формирования стрессорных гранул. Один из обнаруженных нами фрагментов tiRNA – 3′ половинка изотипа аспарагиновой тРНК – по данным кругового дихроизма и ультрафиолетового плавления оказался способен к образованию G-квадруплексов – устойчивых к действию нуклеаз структур, которые, как недавно показано, могут нуклеировать, т.е. инициировать образование стрессорных гранул. Также нами показано, что олигонуклеотиды, имитирующие tiRNA по последовательности, способны индуцировать пути врожденного иммунитета, что в конечном итоге приводит к выработке интерферона бета и может быть связано с активацией воспаления и регуляцией адаптивного иммунитета при старении.
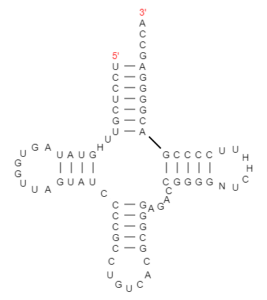
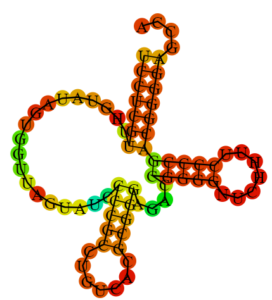
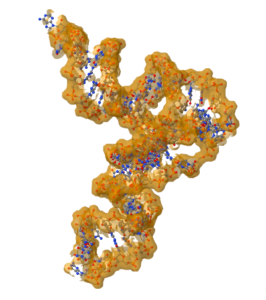
Рис.1 Структуры молекулы тРНК Asp (А) с антикодоном GUC (tdbR00000662) при минимальной свободной энергии (Б), центроидной вторичной структуры (В) и трехмерной конформации (Г), выборка из базы данных [6], расчет вторичных структур с использованием The Vienna RNA Websuite [7].
Рис. 2. Процессинг зрелых форм тРНК с образованием фрагментов-половинок тРНК. Красной огибающей выделены обнаруживаемые фрагменты: А-5’-половинки, Б-3’-половинки.
Рис. 3. Сопоставление фрагментов тРНК в клетках FRSN, подвергнутых хроническому стрессу ЭПР, и репликативно старых FRSN на диаграмме рассеивания, по оси абсцисс и ординат – кратность изменения экспрессии, диаметр точек – логарифм представленности по основанию 2.
Нами с использованием иммунофлуоресценции был проведен анализ внтриклеточного распределения ключевых белков стрессорных гранул G3BP1 и TIA1 в клетках EA.hy926.
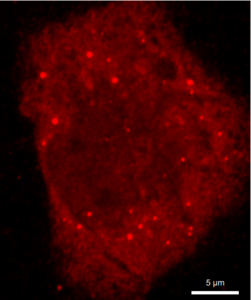
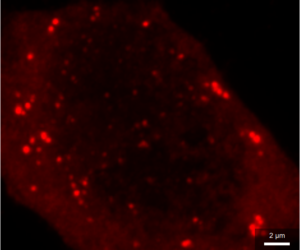
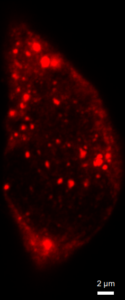
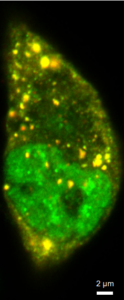
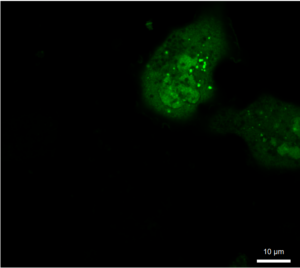
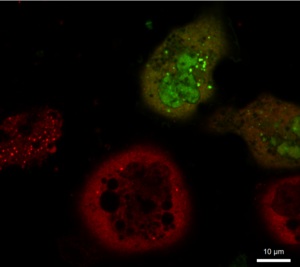
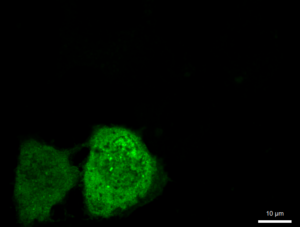
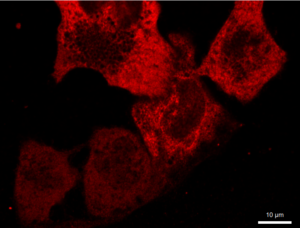
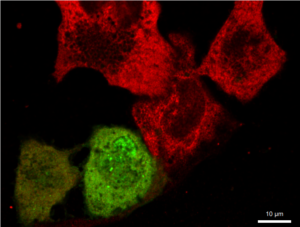
Рис. 4 Микрофотографии меченых анти-G3BP1 антителами клеток EA.hy926, трансфецированных генетической конструкцией с белком TIA1, слитым с GFP
Нами была использована генетическая конструкция, экспрессирующая белок стрессорных гранул TIA1, слитый с GFP. Проверка колокализации этого белка и антител против G3BP1 показала, что в ряде клеток была хорошо выражена ядерная локализация TIA1 наряду с диффузной цитоплазматической (рис.4 А1-3), а в некоторых клетках локализация была преимущественно цитоплазматической (рис.4, Д1-3). В клетках могли присутствовать только TIA1-гранулы (рис.4, Г1-3) при диффузном цитоплазматическом мечении антителами против G3BP1 и отсутствии G3BP1-позитивных гранул. Детектировались также клетки, где присутствовали оба типа гранул без колокализации (рис.4 А1-3), с частичной колокализацией (рис.4 Б1-3) и достаточно высокой степенью колокализации (рис.4 В1-3). Такое разнообразие вариантов может указывать на сложную динамику гранул, их раздельную нуклеацию, слияние, однако, не исключено также влияние артефактов – для уточнения характера возможной коалесценции TIA1-позитивных и G3BP1-позитивных гранул требуется проведение дополнительных исследований.
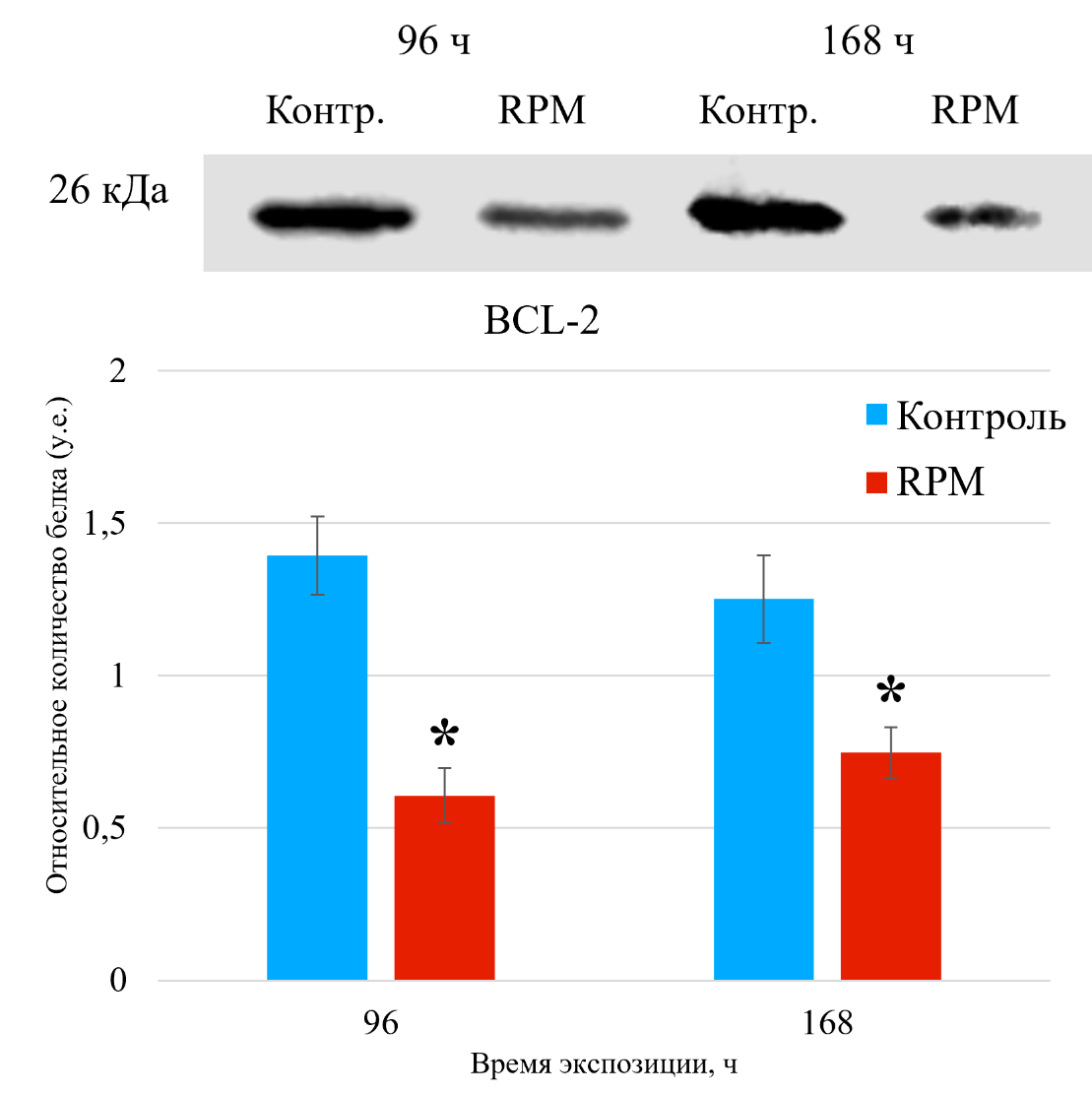
В лаборатории продолжаются исследования влияния микрогравитации на линии клеток. Детально изучены механизмы задержки прогрессии клеточного цикла при RPM-моделированной микрогравитации: уровни белков-циклинов A,B,D,E с помощью вестернблота, иммунофлуоресценции, а также анализа уровней мРНК некоторых их этих циклинов в линии мегариоцитов MEG-01. Снижение уровня мРНК маркера пролиферации Ki-67, а также обнаруженный сдвиг баланса регуляторов в сторону апоптоза может указывать на развитие клеточного стресса в клетках MEG-01, что может иметь важное значение для гомеостаза тканей — приводить к снижению пролиферации клеток в условиях реального космоса и, возможно, уменьшать способность тканей к обновлению.
Рисунок 5. Экспрессия анти-апоптотического белка Bcl-2 в мегакариоцитарных клетках MЕG-01, методом вестерн-блота. Результаты выражены в виде белковых полос и графиков. Данные представлены как средние значения ± стандартное отклонение. *p < 0,05 по сравнению со статическим контролем (n =3).
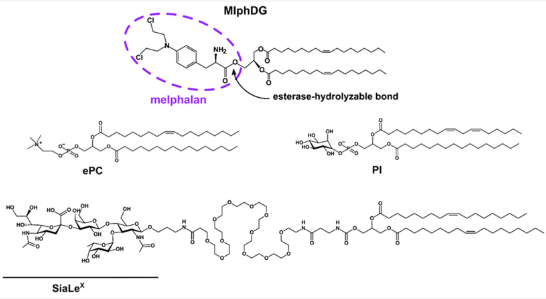
Была впервые изучена интернализация нацеленных на активированный эндотелий липосом при действии на клетки эндотелия варьирующих механических сил, создаваемых засчет контролируемых гидродинамических условий в микрофлюидных чипах. В условиях потока возможны фундаментальные изменения ключевых биохимических процессов – например, кинетики лиганд-рецепторного взаимодействия. Это может повлиять на такие важные для биомедицины процессы, как направленная доставка лекарств к клеткам-мишеням. В этой связи, изучение действия механических сил на клетки, включая их адаптацию, представляется актульным. Мы подвергали эндотелиальные клтки HUVEC в микрофлюидном чипе действию потока с липосомами различного состава для изучения их взаимодействия с клетками в гидродинамических условиях, близких к капиллярному кровотоку, с использованием конфокальной флуоресцентной микроскопии. Включение от 5 до 10% конъюгата лиганта Е-селектина SiaLeX в бислой липосом MlphDG увеличивало их поглощение исключительно активированными эндотелиоцитами как в потоке, так и в статических условиях. Увеличение концентрации сыворотки с 20 до 100% в потоке приводило к снижению поглощения липосом клетками. Чтобы выяснить возможную роль белков плазмы во взаимодействиях липосома-клетка, белковые короны липосом были выделены и проанализированы методами протеомики. Протеомный анализ показал, что постепенное увеличение содержания SiaLeX коррелирует с общим обогащением липосомально-ассоциированных белков несколькими аполипопротеинами, включая наиболее положительно заряженным ApoC1 и сывороточным амилоидом А4, с одной стороны, и снижение содержания связанных иммуноглобулинов, с другой. В статье обсуждается потенциальное вмешательство белков в связывание липосом с селектинами эндотелиальных клеток.
Рисунок 6. Структуры липофильного пролекарства мелфалана (MlphDG), SiaLeX-конъюгата и репрезентативные структуры соевого фосфатидилинозитола (PI) и яичного фосфатидилхолина (ePC), используемых для приготовления липосом.
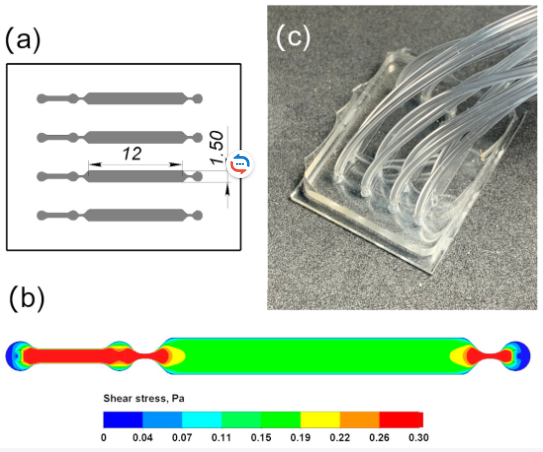
Рис. 7. (а) Схема микрофлюидного чипа: ширина канала 1,5 мм, высота 0,2 мм, длина 12 мм. (b) Тепловая карта распределения напряжения сдвига в канале чипа при объемной скорости 100 мкл/мин. (c) Фотография микрофлюидного чипа.
А Б В Г
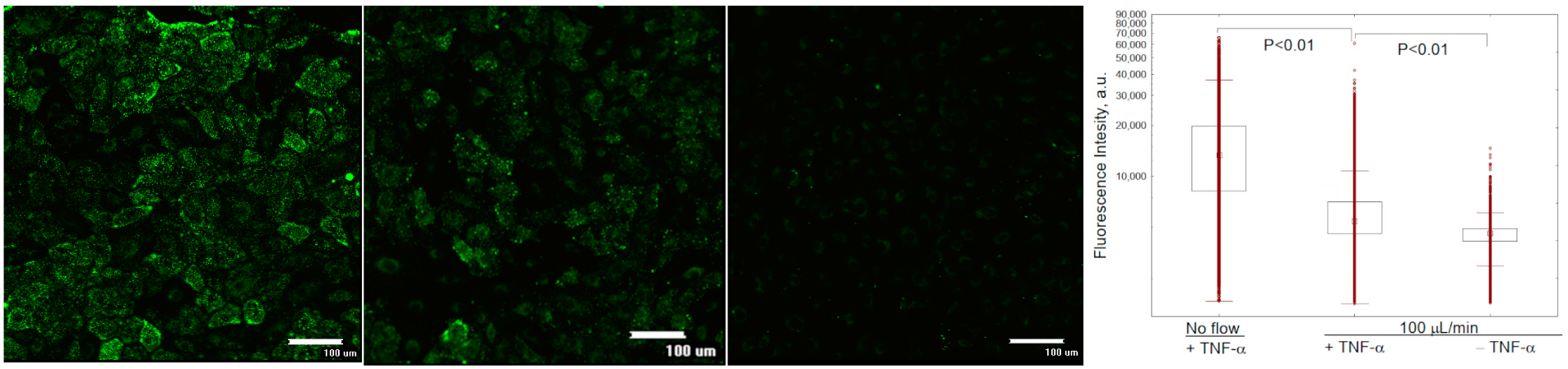
Рисунок 8. Монослой клеток HUVEC, интернализирующих липосомы 5SX. Изображения фрагментов микроканалов с клетками HUVEC после активации в течение 4 ч 50 нг/мл TNF-α: (а) в статических условиях, (б) в потоке 100 мкл/мин или (в) в потоке, без активации. (г) Распределение интенсивности флуоресценции клеток HUVEC, интернализирующих липосомы 5SX; данные по интернализации в статических условиях (НЕТ ПОТОКА) или при скорости потока 100 мкл/мин. Данные представлены в виде медиан, 25–75 процентилей и диапазонов значений без выбросов. Для сравнения групп использовались критерий Краскела-Уоллиса и медианный тест. Монослой клеток, высеянный в микроканалы на 18 часов, активировали в течение 4 часов 50 нг/мл TNF-α. Контрольные клетки не были активированы (-TNF-α). Затем клетки чипа подвергали воздействию потока суспензии липосом во флюоробрайте с 20% FBS в течение 15 мин.
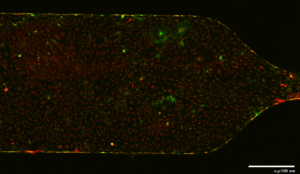
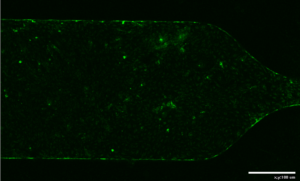
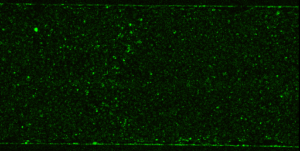
Рис.9 Примеры изображений фрагментов микроканалов микрофлюидного устройства с монослоем клеток HUVEC, активированных в течение четырех часов 50 нг/мл TNF alpha: А,Б – канал №1, 5% SiaLex, 100 мкл/мин: А – зеленая и красная флуоресценции у порта ввода, Б – флуоресценция только BODIPY липосом у порта ввода; В – пример сегментации изображения монослоя,
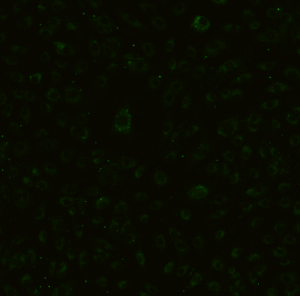
Рис.10 Примеры микроизображений фрагментов микроканалов микрофлюидного устройства с монослоем клеток HUVEC, активированных в течение четырех часов 50 нг/мл TNF alpha: А – левый крайний канал (№1), Б –канал №3 у порта вывода, В,Д – микрофотография активированного эндотелия, интернализующего липосомы с 5% SiaLex, Г,Е — микрофотография неактивированного эндотелия, интернализующего липосомы с 5% SiaLex, стрелками помечены отдельные крупные интенсивно флуоресцирующие клетки предположительно с признаками репликативного старения
А
Б
В
Г
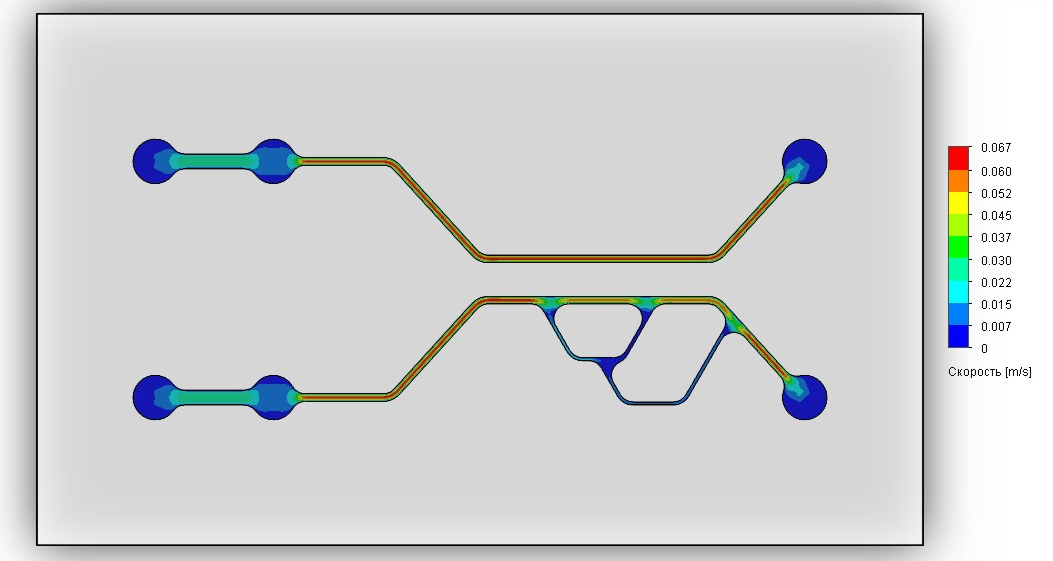
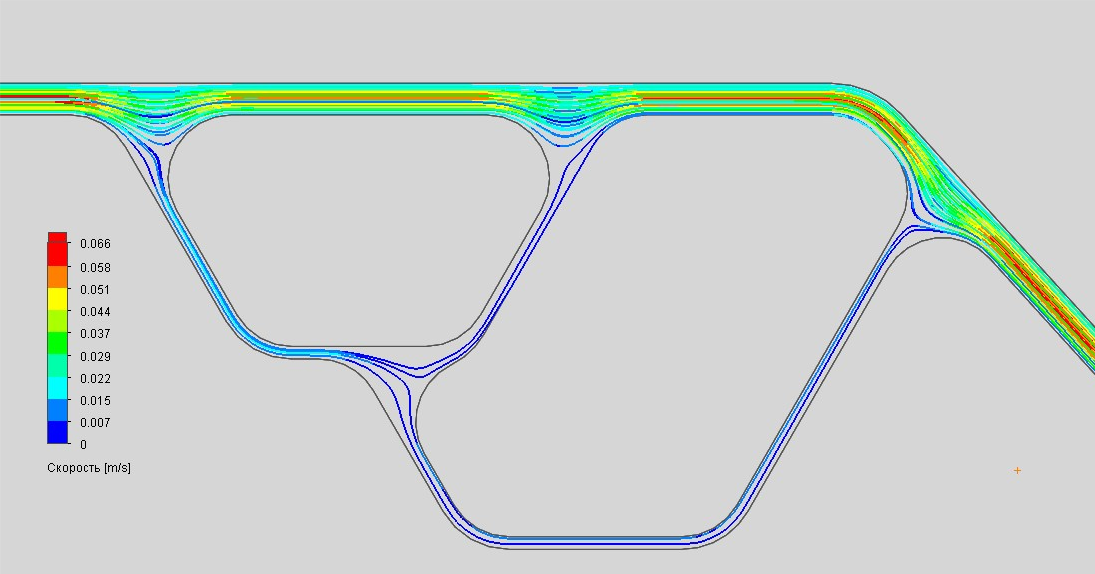
Рис.11 Тепловые карты распределения касательного напряжения (А,Б) и скорости (В,Г) в каналах МФУ, имитирующего аномальную геометрия сосудистого русла, при объемной скорости 100 мкл/мин
В настоящее время помимо государственного задания, лабораторией были выиграны и выполняются несколько грантов:
«Короткие РНК и РНК-деградом при стрессе эндоплазматического ретикулума и стресс-
индуцированном клеточном старении» в рамках гранта РНФ № 22-25-00820
«Персонифицированная микрофлюидная модель дисфункции и старения эндотелия с опорой на генетические данные пациента для оптимизации диагностики и лечения преэклампсии и иных гипертензивных заболеваний» в рамках гранта Фонда научно-технологического развития ХМАО-Югры № 2024-10805/2024 от 30.05.2024 г
Совместный проект с Государственным бюджетным учреждением здравоохранения города Москвы «Детская городская клиническая больница имени З.А. Башляевой Департамента здравоохранения города Москвы» «Частота, факторы риска, клинико-патоморфологические, эндоскопические, морфологические варианты и тактика наблюдения при современном течении колитов у детей с использованием расширенного исследования гемостаза и нового метода жидкостной биопсии и высокопроизводительного секвенирования» ( Договор № 1209-11/25-1НИР на выполнение научно-исследовательских работ с Автономной некоммерческой организацией «Московский центр инновационных технологий в здравоохранении» от 16.05.2025 г).
Некоторые опубликованные статьи:
- Onishchenko, N.R., Moskovtsev, A.A., Kobanenko, M.K., Tretiakova, D.S., Alekseeva, A.S., Kolesov, D. V, Mikryukova, A.A., Boldyrev, I.A., Kapkaeva, M.R., Shcheglovitova, O.N., Bovin, N. V, Kubatiev, A.A., Tikhonova, O. V and Vodovozova, E.L. (2023) Protein Corona Attenuates the Targeting of Antitumor Sialyl Lewis X-Decorated Liposomes to Vascular Endothelial Cells under Flow Conditions. Pharmaceutics, Mol Biol (Mosk), 15. https://doi.org/10.3390/pharmaceutics15061754.
- Dmitry Kolesov, Anna Astakhova, Maria Galdobina, Alexey Moskovtsev, Aslan Kubatiev, Alisa Sokolovskaya, Leonid Ukrainskiy and Sergey Morozov Scanning Probe Microscopy Techniques for Studying the Cell Glycocalyx/ Cells 2023, 12(24), 2778; https://doi.org/10.3390/cells12242778
- Alisa A Sokolovskaya, Mikhail A Popov, Ekaterina A Sergeeva, Arkadiy A Metelkin, Dmitry I Zybin, Dmitry V Shumakov, Aslan A Kubatiev. Investigation of Platelet Apoptosis in Patients after Surgical Myocardial Revascularization. Biomedicines. 2023 Jan 18;11(2):251. doi: 10.3390/biomedicines11020251.
- Sokolovskaya, A., Korneeva, E., Zaichenko, D., Virus, E., Kolesov, D., Moskovtsev, A., & Kubatiev, A. (2020). Changes in the Surface Expression of Intercellular Adhesion Molecule 3, the Induction of Apoptosis, and the Inhibition of Cell-Cycle Progression of Human Multidrug-Resistant Jurkat/A4 Cells Exposed to a Random Positioning Machine. International Journal of Molecular Sciences, 21(3). https://doi.org/10.3390/IJMS21030855
- Kukharsky, M. S., Everett, M. W., Lytkina, O. A., Raspopova, M. A., Kovrazhkina, E. A., Ovchinnikov, R. K., Antohin, A. I., & Moskovtsev, A. A. (2022). Protein Homeostasis Dysregulation in Pathogenesis of Neurodegenerative Diseases. Molecular Biology, 56(6), 967–978. https://doi.org/10.1134/S0026893322060115
- Zaichenko, D. M., Mikryukova, A. A., Astafeva, I. R., Malakho, S. G., Kubatiev, A. A., & Moskovtsev, A. A. (2023). MicroRNA Biogenesis in Cell Senescence Induced by Chronic Endoplasmic Reticulum Stress. Molecular Biology, 57(4), 670–683. https://doi.org/10.1134/S0026893323040192
- Braga, E. A., Burdennyy, A. M., Uroshlev, L. A., Zaichenko, D. M., Filippova, E. A., Lukina, S. S., Pronina, I. v., Astafeva, I. R., Fridman, M. v., Kazubskaya, T. P., Loginov, V. I., Dmitriev, A. A., Moskovtsev, A. A., & Kushlinskii, N. E. (2024). Ten Hypermethylated lncRNA Genes Are Specifically Involved in the Initiation, Progression, and Lymphatic and Peritoneal Metastasis of Epithelial Ovarian Cancer. International Journal of Molecular Sciences, 25(21). https://doi.org/10.3390/IJMS252111843
- Sharipov, R. R., Surin, A. M., Silonov, S. A., Smirnov, E. Y., Neklesova, M. v., Vishnyakov, I. E., Gavrilova, A. A., Mikryukova, A. A., Moskovtsev, A. A., Bakaeva, Z. v., Kolesnikov, S. S., Kuznetsova, I. M., Turoverov, K. K., & Fonin, A. v. (2024). Promyelocytic leukemia protein (PML) knockout increases mitochondrial Ca2+ uptake in HeLa cells. Biochemical and Biophysical Research Communications, 739. https://doi.org/10.1016/J.BBRC.2024.150990
- Фрагменты транспортной РНК при клеточном старении, индуцированном стрессом эндоплазматического ретикулума / Д. М. Зайченко, А. Ю. Пасько, А. А. Микрюкова [и др.] // Патологическая физиология и экспериментальная терапия. – 2024. – Т. 68, № 1. – С. 4-14. – DOI 10.25557/0031-2991.2024.01.4-14. – EDN FFCVGA.
- Cтресс эндоплазматического ретикулума, внеклеточный протеостаз и врожденный иммунитет в патогенезе возрастзависимых заболеваний: болезнь Альцгеймера / Д. М. Зайченко, А. А. Кубатиев, А. А. Москалев, А. А. Московцев // Патологическая физиология и экспериментальная терапия. – 2023. – Т. 67, № 4. – С. 93-102. – DOI 10.25557/0031-2991.2023.04.93-102. – EDN CEKUIG.
- Липополисахариды увеличивают активность IRE1-опосредуемого сигнального пути ответа на гомоцистеин-индуцированный стресс эндоплазматического ретикулума в эндотелиоцитах / А. А. Московцев, А. В. Иванов, Д. М. Зайченко [и др.] // Патологическая физиология и экспериментальная терапия. – 2022. – Т. 66, № 3. – С. 5-18. – DOI 10.25557/0031-2991.2022.03.5-18. – EDN PDDDYC.
- Клеточный стресс, старение и канцерогенез / А. А. Московцев, Д. М. Зайченко, П. К. Иванов, О. Н. Солопова // Патологическая физиология и экспериментальная терапия. – 2023. – Т. 67, № 4. – С. 79-85. – DOI 10.25557/0031-2991.2023.04.79-85. – EDN SSMXZZ.
- Сергеева Е. А., Метелкин А. А., Соколовская А. А. Исследование экспрессии циклинов клеточного цикла в мегакариобластной клеточной линии человека при воздействии моделированной микрогравитации. // Патологическая физиология и экспериментальная терапия. 2023. Т. 67. № 2. С. 17–25. DOI: 10.25557/0031-2991.2023.02.17-25
- Устный доклад — Зайченко Д.М., Московцев А.А.9TH INTERNATIONAL CONGRESS OF PATHOPHYSIOLOGY (International Society of Pathophysiology), July 4 – 7th 2023 in Hotel Crowne Plaza, Belgrade, Serbia. Симпозиум 9, https://isp-belgrade2023.org/
- II Международный форум геномных и биомедицинских технологий «От рождения до активного долголетия», г.Сургут 30 ноября – 2 декабря 2023 Московцев А.А., пленарный устный доклад
- II Международный форум геномных и биомедицинских технологий «От рождения до активного долголетия», г.Сургут 30 ноября – 2 декабря 2023 Московцев А.А., председатель и организатор секции “Микрофлюидика, механобиология и клеточный стресс”.